Messgenauigkeit der blauen Tropfen
Jeder Tropfen der Messflüssigkeit neutralisiert 0,1 ppm bei der Anwendung und entfärbt sich dabei. Nach 10 eingerührten Messtropfen sind also 1 ppm weniger H2-Gas in dem Messbecher mit Wasser. Entfärbt sich nun der 11. Tropfen nicht mehr, dann waren mit Sicherheit mindestens 1 ppm H2-Gas im Wasser gelöst, und mit Sicherheit weniger als 1,1 ppm, weil dann doch zu wenig H2-Gas im Wasser war, um auch noch den 11. Tropfen Methylenblau (ganz) zu entfärben. Die Genauigkeit der Messung ist demnach 1,1 ppm (+ 0 / - 0,1) und das Wasser in diesem Beispiel mit 11 Tropfen hat ein H2-Gehalt zwischen 1,0 und 1,1 ppm (und nicht sicher 1,1 ppm, wie in der Anleitung suggeriert).
Mit dem letzten nicht entfärbten Tropfen wird das Messergebnis also auf den nächst-höheren, aber unwahrscheinlichen 0,1-Schritt (um 0,1 ppm) "aufgerundet".
Das Messergebnis ist aber auch stark von der Größe der Tropfen aus der Pipette abhängig. Größere Tropfen ergeben einen zu kleinen Messwert, und kleinere Tropfen machen das Messergebnis "zu gut".
Nach meinen Laboruntersuchungen bestehen die Tropfen fast oder ganz ausschließlich aus den Komponenten Wasser, 70 % Ethanol, Methylenblau und kolloidalem Platin. Die Größe der Tropfen hängt einerseits von dem Durchmesser der Tropftülle ab, aber andererseits auch besonders von der Oberflächenspannung der abtropfenden Flüssigkeit. (Die Handhabung selbst hat einen geringen Einfluss, wenn die Tropföffnung beim Tropfen immer nach unten zeigt, die Pipette also nicht schräg gehalten wird.). Wasser und Ethanol haben aber eine sehr unterschiedliche Oberflächenspannung (Wasser 72,75 und Ethanol 22,55 mN/m). Das bedeutet: wenn Ethanol (Alkohol) aus der Messflüssigkeit verdunstet, werden die Tropfen größer, es wird mehr H2-Gas je Tropfen neutralisiert, und die Tropfen zeigen einen zu geringen H2-Gehalt im Wasser an. Messtropfen, die längere Zeit offen gestanden sind (oder ggf. auch gegen Ende ihrer Nutzung), zeigen also einen zu niedrigen H2-Gehalt an. Auch wenn die Flasche schon recht leer ist, sammelt sich über der Testflüssigkeit in der Flasche mehr Ethanol-Gas an, welches bei jedem neuerlichen Öffnen der Flasche entweicht.
Wichtig: Nach Beendigung einer Messreihe die Flasche wieder mit dem Original-Dichtpfropfen verschließen und die Pipette auswaschen, denn durch den Gummibalg an der Pipette diffundiert das Ethanol mit der Zeit. Die Messbecher immer sofort nach der Messung ausgießen und solange immer wieder mit Wasser füllen, bis sich das Wasser (über Nacht) nicht mehr blau einfärbt. Dann den Messbecher gründlich mit etwas Wasser und Küchen-Papier ausreiben.
Einfluss der Wasserqualität auf das Messergebnis der blauen Tropfen
Das Messergebnis kann durch im Trinkwasser enthaltene Stoffe beeinflusst werden. Es besteht auch die Möglichkeit, dass die Tropfen bei gewissen Verunreinigungen im Wasser weniger oder sogar überhaupt nichts anzeigen. Solche Stoffe im Wasser, die den Platin-Katalysator deaktivieren können, sind: Blei, Verbindungen der Aminogruppe (Ammoniakderivate wie Chloramine, die zur Wasserdesinfektion verwendet werden), Schwefelverbindungen (Schwefel/Sulfite/Sulfate), Zink, Eisen und Silizium. Das habe ich einmal sehr deutlich erlebt:
In dem Wasser der Bodensee-Wasserversorgung in meinem Büro in Stuttgart z.B. haben die Tropfen zunächst gar kein H2 angezeigt. Schon der erste Tropfen blieb in H2-reichem Wasser blau. Darauf hin habe ich denselben Versuch nochmal mit Wasser aus dem Nachbargebäude wiederholt, und siehe, dort zeigten die Tropfen den erwarteten H2-Gehalt an. Beide Häuser wurden mit derselben Rohrleitung von der Straße aus versorgt, aber in meinem Gebäude waren offensichtlich Stoffe im Leitungssystem, die das Entfärben der Tropfen verhinderten. Nachdem ich dann das Wasser, auf das die Tropfen nicht reagierten, vor dem Boosten mit einem Kannen-Filter gefiltert hatte, der angeblich auch Schwermetalle aus dem Wasser filtert, haben die Tropfen auch in dem Gebäude funktioniert!
Meiner Erfahrung nach zeigen unterschiedliche Wässer auch sonst durchaus kleine Unterschiede, entweder wirklich im H2-Gehalt oder in der Anzeige der Tropfen. Insbesondere unterscheiden sich Wässer darin, wie leicht (schnell) sich H2-Gas im Wasser löst, der maximal erreichbare Sättigungswert unterscheidet sich dagegen kaum oder gar nicht. (siehe Diagramm)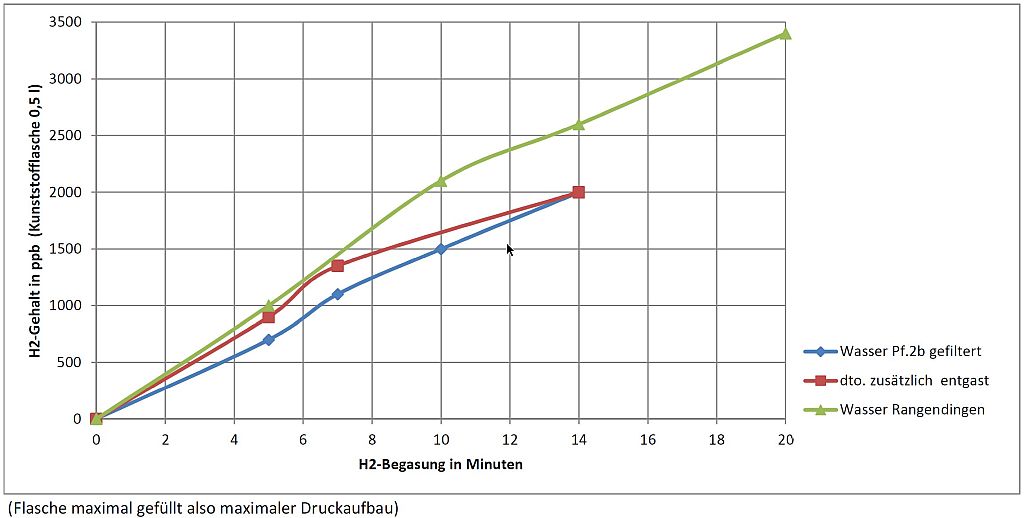
Das Wasser der lokalen Wasserversorgung in Rangendingen löste im Versuch das H2-Gas mit einer Geschwindigkeit von 210 ppb/min, ähnlich dem entlüfteten Bodensee-Wasser Pf.2b,. Bei dem nicht-entlüfteten Bodensee-Wasser Pf.2b betrug die Geschwindigkeit aber nur 150 ppb/min. Verwendet wurde in dem Versuch ein Wasserstoff-Booster (Hibon, SPE H2+) mit 0,5 Liter Mehrweg-Kunststoffflasche aus PET.
Bei dieser Kombination aus Booster und Flasche war der Anstieg des H2-Gehalts nahezu linear (doppelte Begasungsdauer ergibt doppelten H2-Gehalt)
Das entlüftete Wasser erwies sich nur im Anfangsbereich etwas vorteilhafter (und weniger als erwartet). Vermutlich treibt auch das sprudelnde Begasen selbst schon "Fremdgase" aus dem Wasser.
(zur Erklärung: entlüftet nennt man ein Wasser, das keinerlei gelöste Gase enthält. Das kann man durch Abkochen oder durch Vakuumieren erreichen)
Da stellt sich die Frage:
Nimmt unterschiedliches Trinkwasser tatsächlich H2-Gas in unterschiedlicher Weise auf, oder wird die Messung mit den blauen Tropfen von der Wasserqualität beeinflusst?
Schließlich können Schwermetall-Rückstände im Wasser die Reaktion der blauen Tropfen ja auch so stark behindern, dass sie gar kein H2-Gas mehr anzeigen können.
Vergleichsmessungen unterschiedlicher Geräte sollte daher immer nur mit doppelt-destilliertem Wasser erfolgen!
Einfluss der Handhabung auf das Messergebnis der blauen Tropfen
H2-Wasser gibt das gelöste H2-Gas sehr schnell wieder an die Umgebungsluft ab, weil diese ja so gut wie kein H2-Gas enthält, denn Gase haben das Bestreben, sich im Wasser und der umgebenden Atmosphäre in gleicher Konzentration zu verteilen. (Siehe hier: Gasgleichgewicht)
Besonders schnell entweicht das H2-Gas aus dem Wasser, wenn das Wasser schnellen Druckschwankungen ausgesetzt wird. Das Phänomen ist auch von Wasser mit Kohlensäure (Sprudel mit CO2-Gas) oder von Bier und Sekt jedem bekannt: Schüttelt man die Flasche vor dem Öffnen, dann spritzt es, weil die gelöste Kohlensäure durch die mechanische Druckstörung in feinste, unsichtbare Bläschen ausfällt, die dann beim Öffnen die Flüssigkeit heraus-spritzen lassen. Daher:
- Das zu messende Wasser sehr bald nach dem Öffnen der "Booster"-Flasche entnehmen, ohne es zu stören:
- Das Wasser sanft aus geringer Höhe in das Messgefäß schütten, oder besser es mit einer 3 oder 6 ml Einweg-Spritze unter der Wasser-Oberfläche entnehmen. Dabei die Spritze langsam aufziehen und langsam ausdrücken und dabei die Spritzen-Öffnung nahe am Boden oder der Wand des Messgefäßes halten.
- Ist schon bekannt, wie viele Tropfen sich sicher ohne Verfärbung lösen werden, dann diese Tropfenzahl auf einmal ohne Rühren zugeben.
- Damit sich die Tropfen im Wasser verteilen, das Gefäß sanft schwenken, oder mir einem Stäbchen langsam umrühren, ganz nach James Bond Manier:
"... nicht geschüttelt, nur gerührt". - Beim Eintropfen die Pipette so halten, dass die Öffnung der Pipette nicht schräg zur Wasseroberfläche steht (das beeinflusst das Tropfen-Volumen)
- Ganz wichtig: Die Tropfen-Flasche nach jeder Messung schnell wieder verschließen und auf Dauer dazu immer den Original-Verschluss; und nicht die ggf. mitgelieferte Pipette verwenden!
- Weil die Messergebnisse der Tropfen je nach Wasserqualität und Temperatur und geografischer Höhe unterschiedlich ausfallen sollten die Tropfen auf die jeweilige Situation kalibriert werden. Hier beschreibe ich wie das gemacht werden kann. Geht es nur darum zu ermitteln in welchen Wasser gleichen Ursprungs und bei gleicher Temperatur mehr oder weniger H2-Gas enthalten ist, wenn es sich also um einen relativen Vergleich handelt, kann auf die Kalibrierung verzichtet werden.
- Noch besser erscheint es mit nicht mehr (nur) den H2-Gehalt im Wasser in ppm zu bestimmen, sondern die relative H2-Sättigung in % zu ermitteln. Wie das geht, beschreibe ich hier.
Einschätzen der Qualität von H2-Wasser
Das ist es natürlich, worauf es letztlich ankommt! Ziel sollte es sein, dass nach der Zubereitung mehr H2-Moleküle in dem Trinkwasser sind als zuvor, aber dass das Wasser ansonsten unverändert bleibt.
H2-Wasser sollte nach der Anreicherung nicht anders riechen als zuvor, den H2-Gas hat keinen Geruch.
Ein leicht stechender Geruch kann ein Hinweis darauf sein, dass zugleich ggf. unerwünschtes Ozon (O3) durch das Wasser geleitet wurde oder es haben sich andere Moleküle mit einem Eigengeruch gebildet, wie z.B. Chlordioxid (ClO2). Manche "Alternativ-Mediziner" schwören ja auch auf Ozon oder Chlordioxid (sogenanntes MMS = miraculous Mineral Substance) im Trinkwasser, aber beides sind starke Biozide (also: Lebendiges abtötende Substancen), die ich eher als Medikament ansehe, und nicht unbedingt andauernd einnehmen möchte. Bei einer Booster-Flasche kann man im Betrieb am Geräte-Boden riechen, dort tritt bei starken Geräten auch etwas Ozon als Gas aus. Den typischen Ozon-Geruch kann man auch beim Betrieb von Laser-Druckern oder Fotokopierern wahr nehmen, oder in der Nähe von Hochspannungsgeräten.
H2-Wasser sollte auch nicht anders schmecken als zuvor. Obwohl mache die es probieren sagen, es würde etwas weicher schmecken und sie würden mehr davon trinken als von nicht mit H2 aufgeladenem Wasser. Aber das mit Geschmack auch nicht gemeint.. Es sollte nicht metallisch schmecken oder säuerlich etc. Auch ein prickelndes Gefühl im Mund ist untypisch für H2-Wasser.
H2-Wasser sollte natürlich möglichst viele H2-Moleküle enthalten. Es geht ja in erster Linie mal darum, mehr H2 in den Körper zu bekommen. Die gleiche Menge H2 nehme ich mit dem Wasser auf, wenn ich viel Wasser mit geringerem H2-Gehalt, oder weniger Wasser mit höherem H2-Gehalt trinke.
Insofern ist die Qualität von höher angereichertem Wasser nicht an sich besser, aber vielleicht will oder kann ich gar nicht so viel von dem niedriger angereicherten Wasser trinken, wie mir gerade guttäte. Und wie schon anderswo erwähnt, gibt es keine "Überdosis", die ungünstige Nebenwirkung hätte.
Also: viel mehr hilft nicht viel mehr, aber was "genug" ist, mag individuell verschieden sein, und könnte auch von dem Effekt abhängen, der bewirkt werden soll.
Ein Nebel aus feinen Bläschen im H2-Wasser ist kein Qualitätsmerkmal! (warum das so ist, schreibe ich hier)
Wie kann ich abschätzen oder messen wie viel H2-Gas im Wasser gelöst ist?
Leider sind Messgeräte, die man einfach zur Messung ins Wasser halten kann sehr teuer, und der teure Messfühler verbraucht sich auch noch schnell.
Als die genauste Alternative gibt es blaue Messtropfen von verschiedenen Herstellern, mit denen man den H2-Gehalt durch Titration ermitteln kann. Auch diese tiefblaue Tropflösung ist nicht billig, weil sie kolloidales Platin als Katalysator enthält und nur in sehr kleinen Chargen hergestellt wird. Will man jedoch den Gehalt von H2 im Wasser recht genau bestimmen, führt kein Weg an den Tropfen vorbei.
Zur Optimierung von Geräten und aus Forschungsinteresse habe ich sehr viele dieser Flaschen "vertropft", und als Schwabe habe ich mir auch eine Vorgehensweise ausgedacht, wie man mit der Hälfte der Tropfen auch brauchbare Messergebnisse erzielt, wenn der H2-Gehalt in Wasser deutlich über dem Sättigungsgehalt von 1,6 ppm von drucklos bereiteten H2-Wasser liegt. (wie das geht, schreibe ich hier).
Vorsicht ist bei den Tropfen geboten, wenn das zu testende Wasser bestimmte (Schwer-)metalle enthält, den dann zeigen die Tropfen gar nichts mehr an.
Eine ganz grobe Schnellprüfung kann durch Schütteln des H2-Wassers erfolgen. Hat das H2-Wasser mehr als 1,4 bis 1,6 ppm H2-Gehalt gilt es auch drucklos bei Raumtemperatur als übersättigt (so wie Sprudelwasser mit Kohlensäure). Durch ein einmaliges kurzes Schütteln in einer Flasche ohne Überdruck steigt dann ein Teil des gelösten H2-Gases wieder feinperlig an die Oberfläche oder es erscheint schlagartig eine Art Nebel aus sehr feinen Gasbläschen im Wasser. Auch ein Aufschlagen von einem Glas mit übersättigtem H2-Wasser (z.B. auf ein härteres Polster) kann diesen Effekt auslösen. Je höher, übersättigt das Wasser ist, umso empfindlicher reagiert es auf Erschütterungen oder Turbulenzen. Wurde das Wasser unter noch höherem Druck mehrfach übersättigt hergestellt, kann man auch mehrfach einmal kurz schütteln und es kommt dann jedes Mal wieder neues Gas zum Vorschein. Nach einer sehr groben Faustregel gilt, dass jeder einzelne Schüttler den H2-Gehalt im Wasser um ca. 1 ppm reduziert. (muss man etwas üben)
Das H2-Gas kann leider nicht mithilfe eines Laserpointers abgeschätzt werden. Das wurde in einem YouTube-Video als Nachweis empfohlen, aber durch das Laserlicht werden lediglich auch noch sehr feine Gasblasen im Wasser sichtbar, die sonst mit bloßen Augen nicht zu sehen sind. Diese feinsten Gasblasen werden aber auch schon durch den normalen Perlator am Wasserhahn erzeugt, und bleiben sehr lange im Wasser in der Schwebe. Welches Gas in den Bläschen ist, kann nicht erkannt werden und das Vorhandensein eines "Gasnebels" im Wasser ist kein Nachweis für einen hohen H2-Gehalt im Wasser. (Siehe dieses Video mit einem Kreuz-Laser aus dem Baumarkt)
Auch der erreichte Druck im Wasser während der Anreicherung mit H2-Gas ist ein Qualitätsmerkmal, denn wenn reines H2-Gas unter Druck über längere Zeit durch das Wasser perlt und/oder auf der Wasseroberfläche ansteht, so ist der zu erwartende H2-Gehalt im Wasser einzig und alleine von diesem Druck und der Wassertemperatur abhängig. Und solange der Druck erhalten bleibt, bleibt auch die H2-Konzentration im Wasser erhalten. So einfach ist das wirklich, weshalb auch der Druckentwicklung in den Booster-Flaschen oder größeren stationären Geräten die größte Bedeutung zukommt. (Wie man den aktuellen Druck in geschlossenen, durchsichtigen Flaschen trickreich messen kann, beschreibe ich hier.)
Deshalb sollte man die Booster-Flaschen auch immer erst kurz vor dem Trinken öffnen und idealerweise vorher längere Zeit unter Druck belassen. Wobei der Druck in vielen Booster-Flaschen nach Ende der H2-Produktion wieder mit der Zeit abfällt, weil sich noch weiteres Gas im Wasser löst, oder weil die Geräte unter Innendruck etwas undicht sind. Ideal wäre also eine Flasche, die den Druck selbstständig so lange konstant auf dem Maximum hält, bis sie zu Trinken geöffnet wird.
Hier der Zusammenhang zwischen dem Druck in bar bei Raumtemperatur während der Herstellung des H2-Wassers, und der dann maximal erreichbare H2-Gehalt in ppm. In der Praxis liegen die errichten Werte z.T. deutlich darunter, weil das H2-Gas sich anfangs schnell im Wasser löst, aber je näher der H2-Gehalt an die angegebene Sättigungsgrenze kommt, umso langsamer diffundiert weiteres H2 ins Wasser. Auch ist die Geschwindigkeit, mit dem das Wasser das H2-Gas löst, von den sonst noch im Wasser gelösten Stoffen abhängig. Der praxisnäheren Werte in der mittleren Spalte wurden an realem Trinkwasser und nicht an destilliertem und entlüftetem Wasser ermittelt.
| Gas-/Wasser-Druck in bar | erreichter H2-Gehalt nach 6 / 12 min boosten in ppm | maximal erreichbarer H2-Gehalt in ppm |
| 0 (Flasche offen) | 1,3 / 1,5 | 1,57 |
| 1 | 1,8 / 2,8 | 3,15 |
| 2 | 2,4 / 3,8 | 4,72 |
| 3 | 4,0 / 4,5 | 6,29 |
| 4 | noch keine Versuche gemacht | 7,85 |
| 5 | noch keine Versuche gemacht | 9,43 |
Was aber immer stimmt: Verspricht ein Hersteller, dass sein Gerät einen H2-Gehalt entsprechend der rechten Spalte der Tabelle erreicht, aber das Gerät erreicht nicht mindestens den zugehörigen Druck in der linken Spalte, so verspricht er eine Unmöglichkeit. Tatsächlich sollte das Gerät sogar eher einen Druck erreichen, der deutlich über den Tabellenwerten der linken Spalte liegt, denn mit den Tabellenwerten kann der Vorgang der H2-Anreicherung bis zur absoluten Sättigung auch mal mehrere Tage lang dauern. (Der Vorgang ist nicht linear, d.h. Anfangs steigt der Gehalt schnell und dann immer langsamer, und das absolute Maximum zu erreichen kann sehr lange dauern.)
Mit der simplen Technik der Ventil-Flaschen werden bei 2 bar Druck in Glas-Pfandlaschen nach einer Lagerung von 12 h etwa 4 ppm H2-Gehalt erreicht, und nach 40 Tagen Lagerung an die 4,7 ppm H2-Gehalt erreicht.
Einschätzen der Qualität von H2-Badewasser
Beim Baden in wasserstoffreichem Badewasser sollen im Wasser gelöste H2-Gasmoleküle durch die Haut in den Körper diffundieren. H2-Gasbläschen die noch für das Auge sichtbar sind, oder das Badewasser milchig erscheinen lassen, sind zwar vielleicht hübsch anzuschauen, aber sie gelangen nicht durch die Haut in den Körper.
Und selbst wenn neben den sichtbaren H2-Gasbläschen auch noch gelöster Wasserstoff im Badewasser vorhanden ist, liegt der Gehalt an gelöstem H2-Gas dann immer deutlich, oder sogar weit unterhalb der Sättigungsgrenze für H2-Gas im Badewasser (1,4 ppm bei 38 °C).
Hochwertiges H2-Badewasser das mit H2-Gas übersättigt ist muss für das Auge immer absolut klar und blasenfrei sein!
Ob, und wie stark klares Badewasser mit H2-Gas übersättigt ist erkennt man daran, dass sofort ein H2-Gasnebel in Erscheinung tritt, wenn ein scharfer Wasserstrahl unter Wasser in übersättigtes H2-Badewasser eingeleitet wird. Eine derartige, turbulente Störung hat auf das H2-Badewasser denselben Effekt, wie das Schütteln einer bereits geöffneten Sprudelflasche, was das gelöste CO2-Gas sofort schlagartig als Blasen ausfallen lässt.
Damit ist auch klar, dass es keinen aktiven Whirlpool mit H2-Badewasser geben kann!
Blasen im H2-Badewasser bedeuten, dass das Wasser gerade ganz offensichtlich massiv H2-Gas an die Atmosphäre abgibt. Qualitativ hochwertiges, übersättigtes H2-Wasser wird dabei sehr schnell zu "nur" gesättigtem H2-Wasser, wenn es mit H2-Gas durch-sprudelt wird. Wird es aber mit Luft durch-sprudelt, entweicht sehr schnell aller Wasserstoff aus dem Wasser!
Hier ist ein Video das zeigt was passiert, wenn in hochwertiges, übersättigtes H2-Badewasser scharfe Wasserstrahlen aus einem Duschkopf eingeleitet werden. (Die Gas-Bläschen in dem Video kommen nicht aus dem Duschkopf!)


